Trong thông cáo báo chí phát đi hôm 21/12, Tổ chức Y tế Thế giới (WHO) cho biết LightPower iVASARS-CoV-2 1stRT-rPCR Kit - sản phẩm của kit xét nghiệm PCR do công ty Việt Á sản xuất đã nộp hồ sơ chẩn đoán in vitro COVID-19 của WHO EUL (Mã định danh sản phẩm xin phê duyệt khẩn cấp). Mã hồ sơ đăng ký EUL của sản phẩm này là “EUL 0524-210-00”.
"Hồ sơ sản phẩm đã được đánh giá và không đáp ứng được các hồ sơ cần thiết về an toàn, công năng và/hoặc QMS", WHO cho hay.
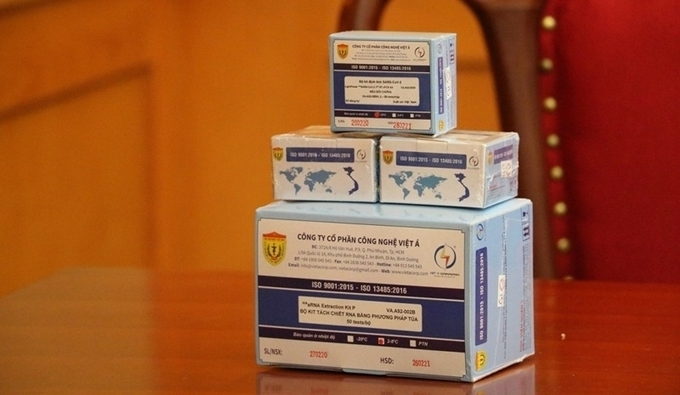
Bộ kit xét nghiệm COVID-19 của Việt Á không được WHO chấp thuận.
WHO có cơ chế tiền kiểm (PQ) để đánh giá tính an toàn, chất lượng và hiệu quả của các sản phẩm y tế thiết yếu bao gồm chẩn đoán in vitro (trong ống nghiệm), thiết bị cắt bao quy đầu cho nam giới, thuốc, vaccine, thiết bị dùng trong tiêm chủng và thiết bị trong dây chuyền lạnh, và sản phẩm kiểm soát vector.
WHO PQ mục tiêu đảm bảo các sản phẩm y tế thiết yếu này sẽ đáp ứng các tiêu chuẩn toàn cầu về chất lượng, an toàn và hiệu quả, nhằm tối ưu hóa việc sử dụng các nguồn lực y tế và cải thiện sức khỏe.
Quy trình PQ cho mỗi dòng sản phẩm được đánh giá một cách minh bạch, khoa học, bao gồm các bước xem xét hồ sơ, thử nghiệm sản phẩm, đánh giá công năng và kiểm tra công tác tổ chức nghiên cứu của cơ sở sản xuất.
Kết quả của PQ bao gồm danh sách các sản phẩm đã được tiền kiểm, danh sách các phòng xét nghiệm đã được tiền kiểm chất lượng và các Báo cáo Kiểm tra và Đánh giá công khai của WHO. Kết quả này được Liên Hợp Quốc và các cơ sở cung ứng khác sử dụng trong quyết định mua bán các sản phẩm y tế.
Ngoài ra, WHO cũng phát triển quy trình Danh sách sử dụng khẩn cấp (EUL) để đẩy nhanh sự sẵn sàng của các sản phẩm y tế quan trọng cần thiết trong tình huống khẩn cấp về sức khỏe cộng đồng.
Quy trình này nhằm hỗ trợ các cơ sở cung ứng và các Quốc gia Thành viên đưa ra các quyết định phù hợp khi sử dụng một IVD cụ thể, dựa trên các dữ liệu tối thiểu về chất lượng, an toàn và công năng có sẵn.
Theo báo cáo công khai về đánh giá sử dụng khẩn cấp của WHO về thiết bị chẩn đoán dịch COVID-19 hôm 20/10/2020, kết quả thẩm định của tổ chức này với bộ kit xét nghiệm COVID-19 của Công ty cổ phần Công nghệ Việt Á là "Không được chấp nhận".
Cụ thể, WHO cho biết bộ kit có tên LightPower iVASARS-CoV-2 1stRT-rPCR Kit của Công ty cổ phần Công nghệ Việt Á - địa chỉ tại phường 9, quận Phú Nhuận, TP.HCM, “không đủ điều kiện để vào chương trình mua sắm của WHO".
Theo WHO, tổ chức này trước đó đã yêu cầu Công ty cổ phần Công nghệ Việt Á cung cấp thông tin cập nhật về tình trạng hệ thống quản lý chất lượng của họ.
Tuy nhiên, các thông tin mà Công ty Việt Nam nộp lại được đánh giá không phải là bằng chứng đầy đủ cho thấy bộ sản phẩm của họ đáp ứng tiêu chuẩn ISO 13485: 2016 đối với thiết bị y tế.







Bình luận